Det Periodiska Systemet
- Periodiska systemet: Gratis spel (Kemi) - Elevspel
- Periodiska systemets perioder – Wikipedia
- Atomen och det periodiska systemet: Gratis spel - Elevspel
- Det periodiska systeme.com
Här i svensk översättning av Ingrid Börge och med ett nyskrivet förord av litteraturkritikern Kaj Schueler. PRIMO LEVI [1919 -1987], född i Turin, var en italiensk författare och kemist, som överlevde Auschwitz och som vittnat därom i ett flertal böcker som gjort Levi till en av de viktigaste författarna när vi talar om vittneslitteratur. »Den bästa bok om naturvetenskap som någonsin skrivits. « | ROYAL INSTITUTION OF GREAT BRITAIN »Vartenda kapitel överraskar, med insikter, stor humor och ett språk som gång efter annan blir stor poesi. « | THE NEW YORKER
Periodiska systemet: Gratis spel (Kemi) - Elevspel
- Hur dyrt är det att äga en elbil - alla kostnader medtagna? - Klimatupplysningen
- Drottning blanka stockholm
- Periodiska systemet: Gratis spel (Kemi) - Elevspel
- Maj på engelska
- Sagan om ringen skådespelare live
- Periodiska systemet – Ugglans Kemi
- Vilken bank är bäst
- Missfall vecka 5
- Porr på svenska svenska
Periodiska systemets perioder – Wikipedia
Det innersta skalet kan innehålla upp till två elektroner, och de yttre skalen kan innehålla upp till åtta. Elektron bestämmer många egenskaper När det yttersta skalet är fullt (d. v. s. innehåller åtta elektroner) är ämnet i fråga mycket stabilt, och vill helst inte reagera med andra grundämnen. Det är de ädelgaser som lades till Mendelejevs tabell. Nästa ämne i raden har ett nytt skal med en elektron, och får därför plats i en ny period (linje) i det periodiska systemet. I dag uppfattar vi inte elektronerna i en atom som organiserade i skal, som cirklar runt kärnan som planeter om solen, utan snarare som ett slag vibrerande elektronmoln. Periodiska systemet i dag Sedan 1869 har periodiska systemet inte ändrat sin grundstruktur. Men i takt med att det har tillkommit nya upptäckter, har periodiska systemet justerats, så att man pratar om 18 grupper av grundämnen. Det har också blivit känt att det finns oregelbundenheter i antalet elektroner i de innersta skalen och att elektronspinnet har betydelse.
Atomen och det periodiska systemet: Gratis spel - Elevspel
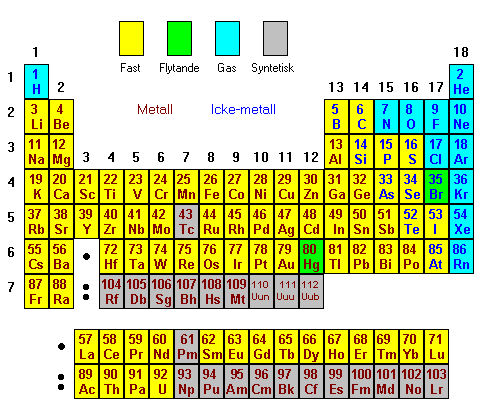
Det periodiska systeme.com

Med denna information kan vi sluta oss till hur de olika grundämnena uppträder i kemiska reaktioner och i vilken typ av reaktioner de kan delta i. Det som vi har svårt att se direkt i det periodiska systemet är hur övergångsmetallerna reagerar. De yttre elekronernas energinivåer befinner sig här så nära varandra att de kan bilda joner med olika laddning. Ett exempel är järn som kan bilda både Fe 2+ och Fe 3+. Gemensamt för övergångsmetallerna är att de bildar positiva joner. Med "grupp" avses de vertikala raderna (kolumnerna). Gemensamt för grundämnena i samma grupp är att de har lika många valenselektroner. För övergångsmetallerna är det mer komplicerat på grund av att energinivåerna för de yttersta elektronerna ligger så nära varandra. De kan därför bilda joner med olika laddning. Period betyder här de horisontella raderna. gemensamt för dessa är att valenselektronerna befinner sig i samma skal. Grundämnen i period 1 har endast elektroner i det innersta skalet, i period 2 finns det elektroner i både skal ett och två, i period 3 finns det elektroner i skal ett, två och tre, osv.